I composti del carbonio sono milioni, perchè in virtù della sua configurazione elettronica si lega con altri atomi di C molto più di qualsiasi altro elemento per formare catene o anelli.
Tutti i composti organici sono composti molecolari.
Ogni atomo di C forma un totale di 4 legami covalenti: con C o altri non metalli, H, alogeni, O o N.
Una caratteristica delle molecole organiche è quella di essere presenti in più forme isomere, cioè composti cohe hanno la medesima formula molecolare, ma diversa struttura (diversa concatenazione degli atomi) o configurazione/conformazione (diversa disposizione nello spazio). Gli isomeri hanno medesimo peso molecolare, ma diverse proprietà chimico-fisiche.
Vi sono due tipi di isomeria:
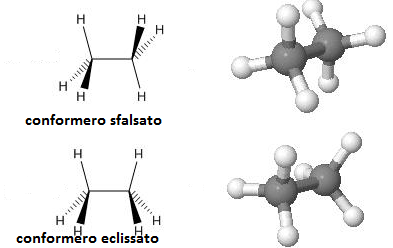
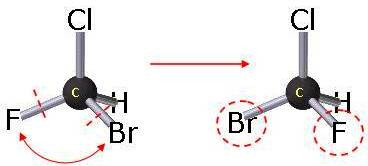
configurazionale: gli isomeri sono converitibili uno nell'altro per rottura e ricostruzione di un legame. (Possono essere diasteroisomeri o enantiomeri):
Gruppi funzionali
In tutte le sostanze organiche, esclusi gli idrocarburi, compaiono una limitata serie di atomi o gruppi atomici ben definiti, chiamati gruppi funzionali.
Ogni gruppo funzionale contraddistingue una specifica famiglia di composti organici con caratteristiche chimico-fisiche comuni.
Meccanismi di reazione delle molecole organiche
Classificazione generale dei reagenti
Meccanismi base delle reazioni organiche
Tipolgia delle reazioni organiche
riduzione= addizione di idrogeno
ossidazione= addizione di ossigeno, rimozione di idrogeno